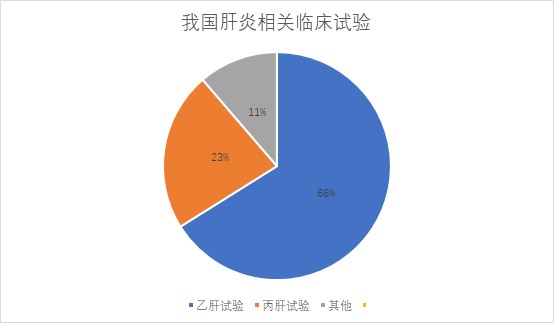
2021年7月28日是第11个世界肝炎日,今年世界卫生组织的宣传主题是“消除肝炎,时不我待”。药研社临床研究数据库的数据显示,2018年1月至2021年7月,我国肝炎相关临床试验总数为292个,其中乙肝与丙肝试验占到89%,乙肝相关193个,丙肝相关66个。目前临床试验目的大多为国内仿制药研发,但同时有多款中国本土创新药表现亮眼。
乙肝药物国产仿制药增加,药物可及性提升
乙肝容易转为慢性,目前尚无有效药物可完全清除乙肝病毒,但经规范的抗病毒治疗,可最大限度抑制病毒复制,延缓和减轻肝脏损害,阻止肝硬化、肝癌及其并发症的发生。
近三年中国乙肝相关临床试验共193个,研究数量排名靠前的两种药物为替诺福韦双索酯和恩替卡韦。两种药物均为国外药企原研:替诺福韦双索酯药物的原研药厂家为吉利德,恩替卡韦药物的原研药厂家为百时美施贵宝公司。
替诺福韦双索酯相关试验共61个,共38家药企进行此类试验,95%为生物等效性试验,其中东阳光集团8个,正大天晴6个。目前市面上已有的国产仿制药厂家有成都倍特、齐鲁制药、正大天晴等。
恩替卡韦原研药厂家为百时美施贵宝,相关试验共29个,95%为生物等效性试验,共23家药企进行此类试验,其中正大天晴3个,其它药企各自1-2个。目前市面上已有的国产仿制药厂家有正大天晴、海南中和等。
值得一提的另一个药物是特拉芬TAF。TAF由吉利德研发,在疗效和安全性上的优势使之成为一线抗乙肝病毒的首选药物,但国内长期没有仿制药,价格高昂。2020年10月19日,成都倍特 4 类仿制药获批上市,成功取得该品种首仿。

进口专利药价格昂贵,一般患者用不起,而国产仿制药的涌现大大增加了药物供给,有效降低药品费用,既减轻患者负担,又使患者能获得更好的治疗效果。
在本土创新药方面,近期乙肝药物研究进展有了重大突破。2021年6月23日,翰森制药(豪森旗下制药公司)艾米替诺福韦片(恒沐®)批准上市,这是我国首个原创口服乙型肝炎新药。相比起第一代替诺福韦,艾米替诺福韦通过优化结构,使得细胞膜穿透率更高,更易进入肝细胞,能更快发挥抗病毒的作用。
丙肝仿制药首上市,本土原研药放光彩
近十年来,随着抗丙肝病毒药物(DAAs)的迅速发展,丙肝已经是可以治愈的疾病。由吉利德研发的索磷布韦就是其中的明星药物。
统计显示,近三年中国丙肝相关临床试验共66个,其中索磷布韦相关试验13个,共有13个药企进行试验。这些试验的目的都很明确——生产仿制药。但截至目前,仅有北京凯因申报的索磷布韦片于2020年3月获得国家药监局批准上市,其它公司尚未走上申报生产。

在丙肝原研创新药方面,近年来我国本土药企交出了值得点赞的答卷。歌礼制药研发的达诺瑞韦钠片(戈诺卫)于2018年6月13日批准上市,成为中国首个本土原研丙肝创新药。北京凯因研发的盐酸可洛派韦胶囊(凯力唯)于2020年1月2日批准上市。东阳光药业研发的磷酸依米他韦于2020年12月22日批准上市。

根据近三年肝炎临床试验数据,我们发现,一方面,随着国家一致性评价的推进和审评审批的加速,仿制药上市的时间被大大缩短,提高了患者的药物可及性。另一方面,在国家鼓励创新药研发的政策支持下,本土药业创新势头迅猛,带来更多适合中国患者的新兴药物。
此次研究由药研社TDC临研数据中心提供支持。药研社临床研究数据库基于国家药品监督管理局药品审评中心等公开信息,将大数据技术与行业知识深度结合,全方位整合临床研究相关领域数据,构建行业知识图谱。作为创新型CRO科技平台,药研社在提供临床研究服务的过程中,通过海量数据辅助临研决策,让药物研发更高效。
(免责声明:本网站内容主要来自原创、合作伙伴供稿和第三方自媒体作者投稿,凡在本网站出现的信息,均仅供参考。本网站将尽力确保所提供信息的准确性及可靠性,但不保证有关资料的准确性及可靠性,读者在使用前请进一步核实,并对任何自主决定的行为负责。本网站对有关资料所引致的错误、不确或遗漏,概不负任何法律责任。
任何单位或个人认为本网站中的网页或链接内容可能涉嫌侵犯其知识产权或存在不实内容时,应及时向本网站提出书面权利通知或不实情况说明,并提供身份证明、权属证明及详细侵权或不实情况证明。本网站在收到上述法律文件后,将会依法尽快联系相关文章源头核实,沟通删除相关内容或断开相关链接。 )